Dalam kimia, rumus empiris atau komposisi kimia dari suatu senyawa kimia adalah ekspresi sederhana jumlah relatif setiap jenis atom (unsur kimia) yang dikandungnya. Suatu formula empiris tidak memberikan gambaran mengenai isomer, struktur, atau jumlah absolut atom. Formula empiris adalah standar bagi senyawa ion, seperti CaCl2, dan makromolekul, seperti SiO2. Istilah "empiris" merujuk pada proses analisis elemental, suatu teknik kimia analitik yang digunakan untuk menentukan persentasi komposisi relatif per unsur dari suatu zat kimia. Kontras dengan formula empiris, formula kimia mengidentikasi jumlah absolut atom unsur-unsur yang ditemukan pada setiap molekul di senyawa tersebut.
Pengertian Rumus Empiris.
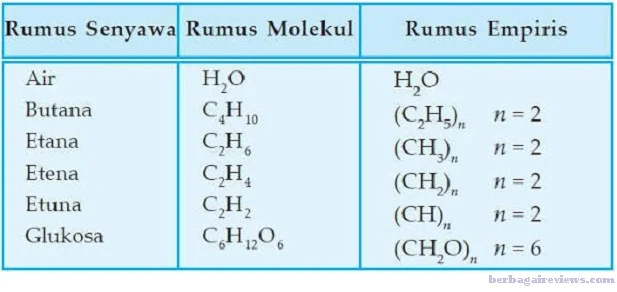
Rumus empiris adalah rumus yang menyatakan perbandingan terkecil atom-atom dari unsur-unsur penyusun senyawa. Sedangkan rumus molekul adalah rumus yang menunjukkan jumlah atom unsur yang menyusun suatu senyawa. Rumus molekul ini merupakan kelipatan dari rumus empiris.
Rumus Molekul, silahkan click http://www.berbagaireviews.com/2018/08/pengertian-rumus-molekul-cara.html
Rumus empiris merupakan rumus yang paling sederhana dari suatu molekul yang menunjukkan perbandingan atom-atom penyusun molekul. Rumus ini menyatakan perbandingan jenis dan jumlah paling sederhana dari suatu senyawa. Rumus empiris diperoleh berdasarkan percobaan. Contohnya, rumus molekul benzena adalah C6H6 dan rumus empirisnya adalah CH. Rumus molekul hidrogen peroksida adalah H2O2 dan rumus empirisnya adalah HO.
(Rumus Empiris)n = Rumus Molekul
Nilai n di atas berkaitan dengan massa molekul relatif (Mr) dari kedua rumus kimia. Jika Mr dari rumus empiris dikalikan dengan n, maka menghasilkan Mr rumus molekul. Prinsip inilah yang dijadikan dasar dalam mencari rumus molekul senyawa.
Rumus empiris dapat digunakan untuk menunjukkan rumus molekul apabila tidak ada informasi tentang massa molekul relatif dari suatu senyawa. Misalnya, NO2 dapat dikatakan sebagai rumus molekul jika tidak ada informasi massa molekul relatifnya. Tetapi jika massa molekul relatifnya diketahui, misalnya 92, maka NO2 merupakan rumus empiris karena rumus molekul senyawa tersebut adalah N2O4.
Cara Menentukan Rumus Empiris.
Pengertian Rumus Empiris.
Rumus empiris adalah rumus yang menyatakan perbandingan terkecil atom-atom dari unsur-unsur penyusun senyawa. Sedangkan rumus molekul adalah rumus yang menunjukkan jumlah atom unsur yang menyusun suatu senyawa. Rumus molekul ini merupakan kelipatan dari rumus empiris.
Rumus Molekul, silahkan click http://www.berbagaireviews.com/2018/08/pengertian-rumus-molekul-cara.html
Rumus empiris merupakan rumus yang paling sederhana dari suatu molekul yang menunjukkan perbandingan atom-atom penyusun molekul. Rumus ini menyatakan perbandingan jenis dan jumlah paling sederhana dari suatu senyawa. Rumus empiris diperoleh berdasarkan percobaan. Contohnya, rumus molekul benzena adalah C6H6 dan rumus empirisnya adalah CH. Rumus molekul hidrogen peroksida adalah H2O2 dan rumus empirisnya adalah HO.
(Rumus Empiris)n = Rumus Molekul
Nilai n di atas berkaitan dengan massa molekul relatif (Mr) dari kedua rumus kimia. Jika Mr dari rumus empiris dikalikan dengan n, maka menghasilkan Mr rumus molekul. Prinsip inilah yang dijadikan dasar dalam mencari rumus molekul senyawa.
Rumus empiris dapat digunakan untuk menunjukkan rumus molekul apabila tidak ada informasi tentang massa molekul relatif dari suatu senyawa. Misalnya, NO2 dapat dikatakan sebagai rumus molekul jika tidak ada informasi massa molekul relatifnya. Tetapi jika massa molekul relatifnya diketahui, misalnya 92, maka NO2 merupakan rumus empiris karena rumus molekul senyawa tersebut adalah N2O4.
Cara Menentukan Rumus Empiris.
- Cari perbandingan massa unsur-unsur penyusun senyawa.
- Cari perbandingan mol dengan membagi massa unsur dengan massa atom relatifnya (Ar).
- Dari perbandingan mol yang paling sederhana didapatkan Rumus Empiris.
- Tentukan Rumus Molekul dengan mencari faktor pengali n. Rumus yang digunakan adalah (Mr RE)n = Mr.
Sebagai contoh, n-heksana, memiliki rumus molekul CH3CH2CH2CH2CH2CH3, menyatakan bahwa senyawa ini memiliki struktur rantai lurus, 6 atom karbon dan dan 14 atom hidrogen. Formula kimia heksana karenanya adalah C6H14, sedangkan rumus empirisnya adalah C3H7 menunjukkan rasio C:H sejumlah 3:7.
Contoh Soal Menentukan Rumus Empiris.
Contoh 1.
Suatu senyawa organik tersusun dari 40 % karbon, 6,6 % hidrogen, dan sisanya oksigen. (Ar C= 12, H=1, O= 16). Jika mr = 90. Tentukan rumus empiris dan rumus molekul senyawa tersebut!
Jawab:
C= 40 %, H= 6,6 %, O = 100 – (40+6,6) = 53,4 %
Mol C : mol H : mol O = 40 / 12 : 6,6 / 1 : 53,4 / 16
= 3,3 : 6,6 : 3,3
= 1 : 2 : 1
jadi, rumus empirisnya adalah CH2O
(CH2O)n = 90
( 1 .Ar C + 2. Ar H + 1. Ar O)n = 90
( 1. 12 + 2. 1 + 1. 16)n = 90
30 n = 90
n = 3
Jadi rumus molekulnya = C3H6O3
Contoh 2.
17 gram suatu oksida logam dengan rumus empiris M2O3 mengandung 8 gram oksigen. Jika Ar O = 16. Berapa Ar logam M tersebut?
Jawab:
Massa O = 8 gram
Massa M = 17 – 8 = 9 gram
Mol M : mol O = 9/ Ar M : 8 / 16 = 2 : 3
Jadi Ar M adalah 27
Contoh 3.
Sebanyak 92 gram senyawa karbon dibakar sempurna menghasilkan 132 gram karbon dioksida dan 72 gram air. Tentukan rumus empiris senyawa tersebut (Ar C = 12, H = 1, dan O = 16).
Jawab:
Massa C = (1. Ar C / Mr CO2 ) x massa CO2 = (12/ 44 ) x 132 gram = 36 gram
Massa H = (2. Ar H / Mr H2O) x massa H2O = (2/ 18 ) x 72 gram = 8 gram
Massa O = 92 – (36 + 8) = 48 gram
Mol C : mol H : mol O = 36/ 12 : 8/ 1 : 48/16 = 3 : 8 : 3
Jadi, rumus empirisnya adalah C3H8O3
Contoh 4
Soal rumus empiris senyawa.
Diketahui:
Persentase unsur C = 41,82% - Persentase unsur H = 6,51% - Persentase unsur O = 51,67%
Ditanya: Rumus empiris?
Jawab:
Massa senyawa sebesar 100 gram, maka:
Massa C = 41,82 gram
Massa H = 6,51 gram
Massa O = 51,67 gram
Kemudian cari jumlah mol masing-masing unsur
Karena perbandingan jumlah mol juga menyatakan perbandingan jumlah atom, maka perbandingan jumlah mol dapat digunakan untuk menentukan rumus empiris.
mol C : mol H : mol O = atom C : atom H : atom O = 3,485 : 6,510 : 3,229
Karena atom-atom dalam molekul merupakan kelipatan bilangan bulat, maka perbandingan atom di atas harus bilangan bulat dan harus lebih sederhana, sehingga harus membagi ketiga bilangan di atas dengan kelipatan bilangan paling kecil yaitu 3,229. Perbandingannya menjadi:
1,07 : 2,01 : 1,00
Perbedaan angka di belakang koma pada desimal kedua dapat diabaikan, dengan demikian perbandingan atom C, H dan O adalah:
1 : 2 : 1
Perbandingan ini menyatakan perbandingan atom-atom paling sederhana dalam molekul. Dengan demikian, rumus empiris senyawa adalah CH2O.




Tidak ada komentar:
Posting Komentar